在社会老龄化和城市化进程加快,以及居民不健康生活方式盛行的背景下,国民心血管病危险因素个体暴露显著增加,导致中国心脑血管病的发病人数持续增加,心脑血管疾病死亡占总死亡人数的 40% 以上,其次是肿瘤[1]。高血压作为心脑血管病最重要的危险因素,而根据2010年第六次全国人口普查数据,测算我国高血压患病人数为2.45亿。近来研究提示高血压与肿瘤之间具有一定的相关性,两者不仅流行病学及病理生理学机制相似,而且两者的危险因素相似,如年龄大、吸烟、糖尿病、高脂血症、肥胖等;高血压本身可能就是肿瘤发生的危险因素,并参与肿瘤发生的过程,且高血压会降低肿瘤患者的总体生存率[2],因此肿瘤患者与普通高血压患者相比,更应该注重高血压的防治。

1、 引起高血压的肿瘤
嗜铬细胞瘤(pheochromocytoma ,PHEO)是起源于肾上腺髓质嗜铬细胞的神经内分泌肿瘤 ,肾上腺外来源的PHEO称为副神经节瘤(paraganglioma ,PGL),主要临床表现为高儿茶酚胺分泌所致的高血压及其并发症,由于肿瘤持续性或阵发性分泌释放不同比例的肾上腺素和去甲肾上腺素,故患者的临床表现不同,典型的临床表现有高血压、头痛 、出汗和心悸等,严重者可导致高血压危象 、心力衰竭 、心肌病和心肌梗死等,危及生命。嗜铬细胞瘤确诊后进行手术治疗,既切除了肿瘤,也治愈了继发性高血压。因此早期诊断并合理治疗尤为重要。
肾素瘤(reninoma)又称肾球旁细胞瘤,是一种罕见的以分泌肾素为特征的肾内良性肿瘤。肾素瘤常见于青年人,典型表现有高血压、低血钾综合征和血浆肾素活性及醛固酮水平增高。部分患者由于严重高血压会出现头痛、恶心、呕吐等高血压脑病的表现,也有少数患者血压正常。肾素瘤确诊需要术后病理结果,虽然该肿瘤是良性肿瘤,但由于伴随高血压和低血钾也会导致严重的并发症。
垂体瘤是最常见的中枢神经系统肿瘤之一,在一般人群中垂体瘤的发病率高达16.7%[3]。瘤体若发展为较大的腺瘤,从而产生占位效应,压迫导水管可出现头痛、恶心、呕吐等颅内压升高症状,此外功能性垂体瘤分泌过多的泌乳素、生长激素、促甲状腺激素等,引起患者血压升高。手术治疗是许多垂体瘤的首选治疗。
分泌醛固酮的肾上腺皮质癌是原发性醛固酮增多症的罕见类型,其肾上腺皮质分泌过量醛固酮,导致体内潴钠排钾,血容量增多,肾素-血管紧张素系统活性受抑。临床主要表现为高血压伴低血钾。研究发现,醛固酮过多是导致心肌肥厚、心力衰竭和肾功能受损的重要危险因素,与原发性高血压患者相比,原醛症患者心脏、肾脏等高血压靶器官损害更为严重。因此,早期诊断、早期治疗就显得至关重要。
2、 抗血管生成靶向药与高血压
肿瘤组织中的血管发生是肿瘤细胞增殖、侵袭、转移的基础,抗血管生成靶向药物能够显著提高抗肿瘤疗效,延长患者生存,在肿瘤治疗中得到广泛应用。高血压作为靶向抗肿瘤药物常见的副作用之一,严重时不得不使患者增加降压药物或者减量甚至终止靶向抗肿瘤药物,其诱导高血压的机制包括:导致NO的产生减少、内皮素-1分泌增多、微血管稀疏化、氧化应激增加、细胞内游离钙离子浓度增加、肾损伤等[4]。有研究认为高血压可能是预测抗血管生成靶向药物疗效的生物标记,但也有回顾性研究结果显示,高血压的发生与肿瘤患者预后并无相关性,高血压是否可作为肿瘤患者抗血管生成靶向药物疗效生物标记尚存在争议,需更多前瞻性的临床试来验证[5, 6]。
3、肿瘤患者的血压评估
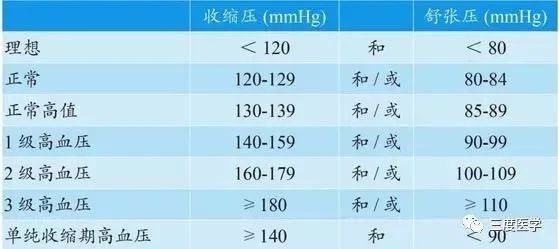
《中国高血压防治指南2018年修订版》将高血压定义为:在未使用降压药物的情况下,非同日3次测量诊室血压,收缩压≥140mmHg 和(或) 舒张压≥90mmHg;患者既往有高血压史,目前正在使用降压药物,血压虽然低于140/90mmHg,仍应诊断为高血压;动态血压的高血压诊断标准为: 平均收缩压/舒张压24h≥130/80mmHg;白天≥135 /85mmHg;夜间≥120/70mmHg。部分患者抗肿瘤靶向药物治疗期间发生高血压的评估,还应参照美国国立癌症研究所(National Cancer Institute,NCI) 制订的通用不良反应术语标准 (Conmon terminology criteria for adverse events,CTCAE v5.0)分级,最新的5.0版本成人分级具体如下:1级,收缩压120~139mmHg,或(和)舒张压80~89mmHg;2级,如果既往在正常值范围内,收缩压140~159mmHg,或(和)舒张压90~99mmHg;反复或持续性(≥24 小时)舒张压升高>20 mmHg或血压大于140/90mmHg;需要给予单药治疗;3级,收缩压≥160mmHg,或(和)舒张压≥100mmHg;需要医学干预,甚至需要多种药物治疗或强化治疗;4级,危及生命(如恶性高血压,一过性或持久性神经功能受损,高血压危象);需要紧急治疗;5级,死亡。
4、肿瘤患者的降压治疗
对于普通高血压患者,根据危险分层不同,由改善生活方式衔接到启动药物治疗的过度观察期可从数周至1-3月,而服用靶向抗肿瘤药物的患者高血压往往与靶向药物程剂量依赖性,尽早的药物干预治疗可降低抗血管生成靶向药的中断率,更有效预防或延迟脑卒中、心肌梗死、心力衰竭、肾功能不全等并发症发生,其血压监测与评估更为重要。一般患者血压目标需控制到140/90mmHg 以下,在可耐受和可持续的条件下,其中部分有糖尿病、蛋白尿等的高危患者的血压可控制在130/80mmHg以下;65~79岁的普通老年人,血压≥150/90mmHg时推荐开始药物治疗;≥80岁的老年人SBP≥160mmHg时开始药物治疗。
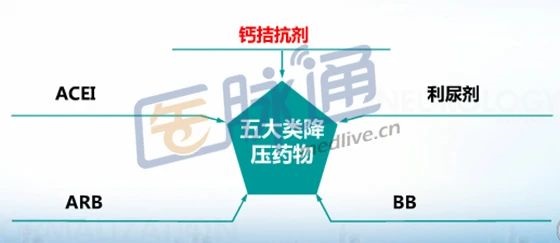
常用降压药物包括钙通道阻滞剂(CCB) 、血管紧张素转化酶抑制剂(ACEI)、血管紧张素受体拮抗剂 ARB、利尿剂和β受体阻滞剂五类,以及由上述药物组成的固定配比复方制剂。血压控制达标是这些降压药物减少心脑血管并发症的最主要原因,而药物之间的差别总体很小,五大类降压药物均可作为初始和维持用药的选择,应根据患者的危险因素、亚临床靶器官损害以及合并临床疾病情况,合理使用药物,优先选择某类降压药物。单片复方制剂是由不同作用机制的两种或两种以上的药组成,是联合治疗的新趋势,尤其适合高血压、肿瘤等慢性病患者。ACEI/ARB与利尿剂或钙拮抗剂联合是高血压单片复方制剂的常用联合方案,可改善治疗的依从性及疗效,并可互相抵消或减轻不良反应。
5、小结
高血压不仅会降低肿瘤患者的总体生存率,也能影响肿瘤患者抗血管生成靶向药的长有效治疗剂量、疗程,而且部分恶性肿瘤的临床表现之一就是高血压,因此肿瘤患者与普通高血压患者相比,血压的监测、评估和治疗更为重要。降压时机以及药物的选择应个体化,要结合危险因素、临床靶器官损害以及合并临床疾病情况。单片复方制可改善治疗的依从性及疗效,是联合治疗的新趋势,尤其适合高血压、肿瘤等慢性病患者。
参考文献
[1]国家心血管病中心. 中国心血管病报告2018[M]. 北京: 中国大百科全书出版社, 2018.
[2]陈琦玲. 特殊类型高血压临床诊治要点专家建议[J]. 中国全科医学, 2020,23(10):1202-1228.
[3]Bettegowda C. Pituitary adenomas: historical perspective, surgical management and future directions[J]. Cns
Oncology, 2015,4(6):411-429.
[4]Maitland M L, Bakris G L, Black H R, et al. Initial Assessment, Surveillance, and Management of Blood Pressure in
Patients Receiving Vascular Endothelial Growth Factor Signaling Pathway Inhibitors[J]. Jnci Journal of the National
Cancer Institute, 2010(9):9.
[5]Therasse P, Arbuck S G, Eisenhauer E A, et al. New Guidelines to Evaluate the Response to Treatment in Solid
Tumors[J]. Journal of the National Cancer Institute, 2000,92(3):205-216.
[6]Rixe O, Billemont B, Izzedine H. Hypertension as a predictive factor of Sunitinib activity[J]. Annals of
Oncology, 2008,18(6):1117.